Suyun Benzersiz Özellikleri
Su, çoğu tortul kayanın oluşumunda rol oynar. Kimyasal tortul kayalardaki minerallerin oluşumunda rol oynayan ana etkenlerden biridir. Aynı zamanda detrital tortul kayaç haline gelen taneleri üreten bir ayrışma ve erozyon maddesidir. Bazı özel nitelikler suyu özellikle eşsiz bir madde haline getirmekte ve tortu ve tortul kayaç üretiminin ayrılmaz bir parçası yapmaktadır.
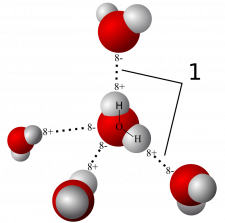
Su molekülü, özel ve önemli bir geometride düzenlenmiş bir oksijen atomuna kovalent olarak bağlanmış iki hidrojen atomundan oluşur. İki hidrojen atomu yaklaşık 105 derecelik bir açı ile ayrılır ve her ikisi de oksijen atomunun bir tarafında bulunur. Bir tarafta pozitif yüklü hidrojenler ve diğer tarafta negatif yüklü oksijenin bulunduğu bu atomik düzenleme, su molekülüne polarite adı verilen bir özellik kazandırır. Bir pili veya mıknatısı andıran molekülün pozitif-negatif mimarisi, bir dizi benzersiz özelliğe yol açıyor.
Polarite, su moleküllerinin diğer maddelere yapışmasını sağlar. Buna adezyon denir. Su aynı zamanda kohezyon adı verilen bir özellik olarak kendi kendine de çekilir ve bu da suyun havadaki en yaygın formu olan damlacığa yol açar. Kohezyon, çeşitli böceklerin ağırlıklarını yüzeye dağıtarak su üzerinde yürümek için kullandıkları yüzey geriliminin yaratılmasından sorumludur.
Suyun kendi kendini çekmesi, doğal dünyada son derece nadir görülen bir başka önemli özelliğe yol açar: sıvı form katı formdan daha yoğundur. Suyun polaritesi, hidrojen bağları adı verilen özel bir zayıf bağ türü yaratır. Hidrojen bağları sıvı su içindeki moleküllerin birbirine yakın durmasını sağlar. Su 4°C'de en yoğundur ve bu sıcaklığın üstünde ve altında daha az yoğundur. Su katılaşıp buza dönüşürken, moleküllerin kristal kafese sığmak için birbirinden uzaklaşması gerekir, bu da suyun genişlemesine ve donarken daha az yoğun hale gelmesine neden olur. Bu nedenle buz yüzer ve 4oC'deki su batar, bu da okyanusları sıvı halde tutar ve aşağıdan yukarıya doğru donmalarını önler. Suyun bu eşsiz özelliği, su gezegeni olan Dünya'yı yaşanabilir kılmaktadır.
Yaşamı desteklemek için daha da kritik olan su, çok geniş bir sıcaklık aralığında sıvı halde kalır ve bu da kohezyonun bir sonucudur. Hidrojen bağı, sıvı suyun buhar veya gaza dönüşmeden önce yüksek miktarda enerji emebilmesini sağlar. Suyun sıvı olarak kaldığı geniş aralık olan 0°C-100°C (32°F-212°F), diğer maddelerde nadiren görülür. Bu yüksek kaynama noktası olmasaydı, bildiğimiz sıvı su Dünya'da dar sıcaklık bölgelerine sıkışırdı, bunun yerine su kutuptan kutba bulunur. Ayrıca su, Dünya'nın yüzey ortamlarında katı, sıvı ve gaz olmak üzere her üç fazda da bulunan tek maddedir.
Su evrensel bir çözücüdür, yani yaygın olarak bulunan, doğal olarak oluşan diğer sıvılardan daha fazla maddeyi çözer. Su molekülleri, iyonları kristal kafesten uzaklaştırmak için polarite ve hidrojen bağlarını kullanır. Su o kadar güçlü bir çözücüdür ki, yeterli zaman verildiğinde en güçlü kaya ve mineralleri bile çözebilir.
Önceki Ders: Ayrışma, Erozyon ve Tortul Kayaçlar
Önceki Ders: Ayrışma ve Aşınma



Yorumlar
Yorum Gönder