Hücre Büyümesi ve Bölünmesi
Bu bölümde şimdiye kadar birçok kez hücre bölünmesinin önemini ve yaygınlığını okudunuz. Vücutta hücre bölünmesine uğramayan birkaç hücre olsa da (gametler, kırmızı kan hücreleri, çoğu nöron ve bazı kas hücreleri gibi), somatik hücrelerin çoğu düzenli olarak bölünür. Somatik hücre, vücut hücresi için kullanılan genel bir terimdir ve yumurta ve sperm üreten hücreler hariç (bunlar üreme hücreleri olarak adlandırılır) tüm insan hücreleri somatik hücrelerdir. Somatik hücreler, kromozomlarının her birinin iki kopyasını içerir (her ebeveynden bir kopya alınmıştır). Homolog bir kromozom çifti, her somatik hücrede bulunan tek bir kromozomun iki kopyasıdır. İnsan diploid bir organizmadır ve somatik hücrelerin her birinde 23 homolog kromozom çifti bulunur. Kromozom çiftlerine sahip olma durumu diploidi olarak bilinir.
Vücuttaki hücreler bir insanın yaşamı boyunca kendilerini yenilerler. Örneğin, gastrointestinal sistemi kaplayan hücreler, gıdaların bağırsaklardaki hareketi nedeniyle sürekli olarak "aşındığında" sık sık yenilenmelidir. Peki bir hücrenin bölünmesini ne tetikler ve hücre bölünmeye nasıl hazırlanır ve bölünmeyi nasıl tamamlar? Hücre döngüsü, bir önceki hücre bölünmesi döngüsünün sonunda yaratıldığı andan, daha sonra kendini bölerek iki yeni hücre oluşturana kadar hücrenin yaşamındaki olaylar dizisidir.
Hücre Döngüsü
Hücre döngüsünün bir "dönüşü" veya döngüsü iki genel aşamadan oluşur: interfaz, ardından mitoz ve sitokinez. İnterfaz, hücre döngüsünün hücrenin bölünmediği dönemidir. Hücrelerin çoğunluğu çoğu zaman interfazdadır. Mitoz, hücre çekirdeğinin parçalandığı ve iki yeni, tamamen işlevsel çekirdeğin oluştuğu genetik materyalin bölünmesidir. Sitokinez sitoplazmayı iki farklı hücreye böler.
İnterfaz
Bir hücre G1 adı verilen dönemde büyür ve tüm normal metabolik işlevleri ve süreçleri yerine getirir (aşağıdaki şekil). G1 fazı (boşluk 1 fazı) hücre döngüsündeki ilk boşluk veya büyüme fazıdır. Tekrar bölünecek hücreler için G1'i S fazı sırasında DNA'nın kopyalanması takip eder. S fazı (sentez fazı), bir hücrenin DNA'sını kopyaladığı dönemdir.
Sentez aşamasından sonra hücre G2 aşamasına geçer. G2 fazı, hücrenin büyümeye devam ettiği ve mitoz için gerekli hazırlıkları yaptığı ikinci bir boşluk fazıdır. G1, S ve G2 evreleri arasında, hücreler en çok G1 evresi sürelerinde değişiklik gösterecektir. Bir hücre burada birkaç saat ya da günlerce kalabilir. S fazı tipik olarak 8-10 saat arasında, G2 fazı ise yaklaşık 5 saat sürer. Bu evrelerin aksine, G0 evresi hücre döngüsünün dinlenme evresidir. Bölünmeyi geçici olarak durduran ve dinlenmekte olan hücreler (yaygın bir durum) ve bölünmeyi kalıcı olarak durduran hücrelerin (sinir hücreleri gibi) G0'da olduğu söylenir.
Kromozomların Yapısı
İnsan vücudunda her gün milyarlarca hücre bölünmektedir. İnterfazın sentez fazı (DNA sentezi için S) sırasında, hücre içindeki DNA miktarı tam olarak iki katına çıkar. Bu nedenle, DNA kopyalanmasından sonra ancak hücre bölünmesinden önce, her hücre aslında her kromozomdan iki kopya içerir. Kromozomun her bir kopyası kardeş kromatid olarak adlandırılır ve diğer kopyaya fiziksel olarak bağlıdır. Sentromer, bir kardeş kromatidi diğerine bağlayan yapıdır. Bir insan hücresi 46 kromozoma sahip olduğundan, bu aşamada hücrede 92 kromatid (46 × 2) vardır. Bir çift kromatid (bir kromozom ve mitoz bölünme sırasında eklenen tam kopyası) ile homolog kromozom çifti (her ebeveynden bir tane olmak üzere ayrı ayrı kalıtılan iki eş kromozom) kavramını karıştırmadığınızdan emin olun (Şaşağıdaki şekil).
Mitoz Bölünme ve Sitokinez
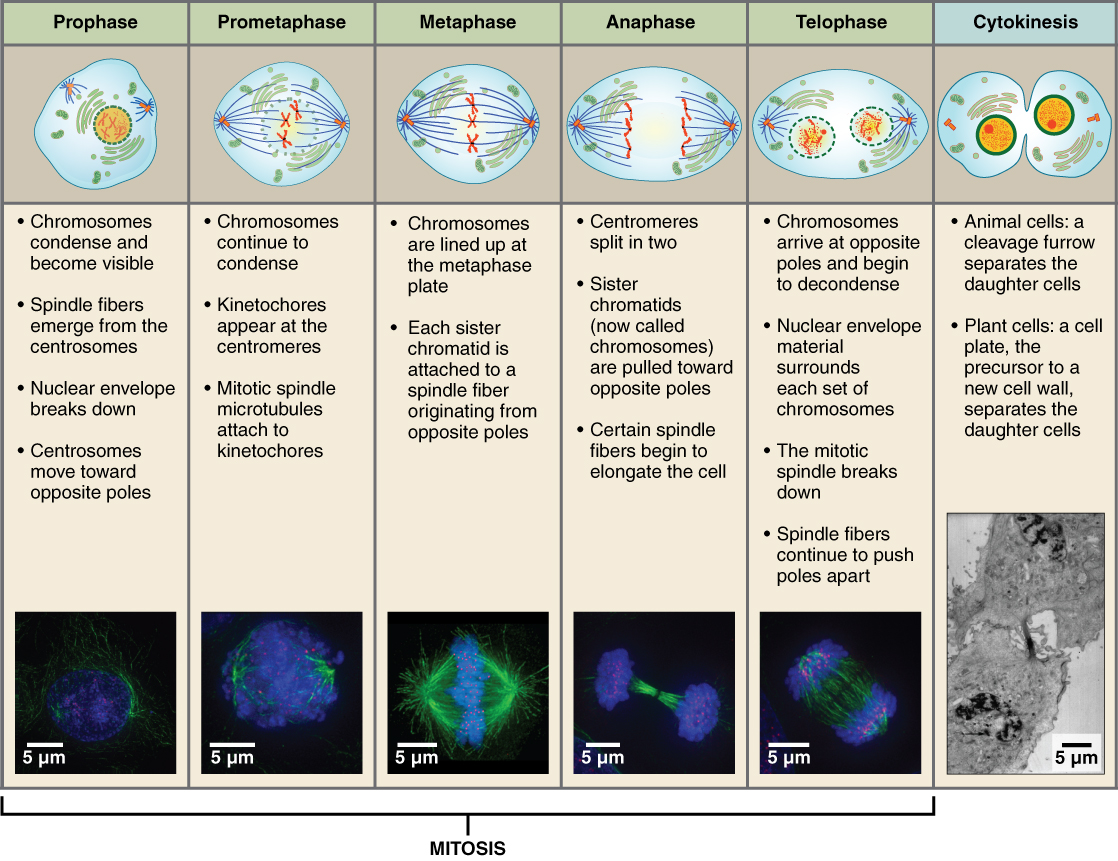
Hücrenin mitotik fazı tipik olarak 1 ila 2 saat arasında sürer. Bu aşamada, bir hücre iki ana süreçten geçer. İlk olarak, -çekirdeğin içeriğinin eşit bir şekilde ayrıldığı ve iki yarısı arasında dağıtıldığı- mitoz bölünmeyi tamamlar. Daha sonra sitokinez gerçekleşerek sitoplazma ve hücre gövdesi iki yeni hücreye bölünür. Mitoz, interfazdan sonra (aşağıdaki şekil) ve şu sırayla gerçekleşen dört ana aşamaya ayrılır: profaz, metafaz, anafaz ve telofaz. Süreci daha sonra sitokinez takip eder.
Profaz, mitozun ilk aşamasıdır ve bu sırada gevşek bir şekilde paketlenmiş kromatin sarmallanır ve görünür kromozomlar halinde yoğunlaşır. Profaz sırasında, her kromozom benzer partnerine bağlanarak görünür hale gelir ve kardeş kromatidlerin tanıdık X şeklini oluşturur. Nükleolus bu evrenin başlarında kaybolur ve nükleer zarf da parçalanır.
Profaz sırasında meydana gelen önemli bir olay, mikrotübül büyümesi için başlangıç bölgesini içeren çok önemli bir yapıyla ilgilidir. Mikrotübüllerin uzandığı çıkış noktaları olarak görev yapan sentriyol adı verilen hücresel yapıları hatırlayın. Bu küçük yapılar mitoz bölünme sırasında da çok önemli bir rol oynar. Sentrozom bir çift sentriyolün bir araya gelmesidir. Hücre, profaz sırasında birbirinden ayrılmaya başlayan yan yana iki sentrozom içerir. Sentrozomlar hücrenin iki farklı tarafına göç ederken, mikrotübüller birbirlerine doğru uzanan iki elin uzun parmakları gibi her birinden uzanmaya başlar. Mitotik iğ, sentrozomlardan ve onların ortaya çıkan mikrotübüllerinden oluşan yapıdır.
Profazın sonuna doğru, mitotik iğden gelen mikrotübüller tarafından nükleer alanın istilası söz konusudur. Nükleer membran parçalanmıştır ve mikrotübüller kendilerini kardeş kromatid çiftlerine bitişik olan sentromerlere bağlar. Kinetokor, mitotik iğ ile kardeş kromatidler arasındaki bağlantı noktası olan sentromer üzerindeki bir protein yapısıdır. Bu aşama, profaz ve metafaz arasındaki geçişi belirtmek için geç profaz veya "prometafaz" olarak adlandırılır.
Metafaz, mitoz bölünmenin ikinci aşamasıdır. Bu aşamada kardeş kromatidler, bağlı mikrotübülleriyle birlikte hücrenin ortasında doğrusal bir düzlem boyunca sıralanır. Artık hücrenin her iki ucunda bulunan sentrozomlar arasında bir metafaz plakası oluşur. Metafaz plakası, kardeş kromatidlerin üzerinde konumlandığı iğin merkezinden geçen düzleme verilen addır. Şimdi mikrotübüller, kardeş kromatidleri ayırmak ve her çiftin bir tanesini hücrenin her iki tarafına getirmek için hazır durumdadır.
Anafaz, mitoz bölünmenin üçüncü aşamasıdır. Anafaz, kardeş kromatid çiftlerinin birbirinden ayrılarak bir kez daha ayrı kromozomlar oluşturduğu birkaç dakika içinde gerçekleşir. Mikrotübüller kısaldıkça bu kromozomlar kinetokorları tarafından hücrenin karşıt uçlarına çekilir. Hücrenin her bir ucu, her bir kardeş kromatid çiftinden bir eş alarak iki yeni yavru hücrenin aynı genetik materyali içermesini sağlar.
Telofaz, mitoz bölünmenin son aşamasıdır. Telofaz, bölünen hücrenin her iki ucunda iki yeni yavru çekirdeğin oluşmasıyla karakterize edilir. Yeni oluşan bu çekirdekler genetik materyalin etrafını sarar ve kromozomlar gevşek bir şekilde paketlenmiş kromatine dönecek şekilde çözülür. Nükleoller de yeni çekirdeklerin içinde yeniden ortaya çıkar ve mitotik iğ birbirinden ayrılarak her yeni hücre kendi DNA, organel, membran ve sentriyol tamamlayıcısını alır. Bu noktada, sitokinez başlarken hücre zaten ikiye bölünmeye başlamıştır.
Yarılma oluğu, sitokinez sırasında hücrenin orta çizgisi etrafında oluşan mikrofilamentlerden oluşan kontraktil bir banttır. (Mikrofilamentlerin aktinden oluştuğunu hatırlayın). Bu kasılma bandı iki hücreyi birbirinden ayrılana kadar sıkıştırır. Şimdi iki yeni hücre oluşmuştur. Bu hücrelerden biri ("kök hücre") kendi hücre döngüsüne girer; gelecekteki bir zamanda tekrar büyüyebilir ve bölünebilir. Diğer hücre dokunun işlevsel hücresine dönüşür ve tipik olarak oradaki "eski" bir hücrenin yerini alır.
Mitozu tamamlamış ancak sitokinez geçirmemiş bir hücre düşünün. Bazı durumlarda, bir hücre genetik materyalini bölebilir ve boyut olarak büyüyebilir, ancak sitokinez geçiremez. Bu, birden fazla çekirdeğe sahip daha büyük hücrelerle sonuçlanır. Genellikle bu istenmeyen bir sapmadır ve kanserli hücrelerin bir işareti olabilir.
Hücre Döngüsü Denetimi
Çok ayrıntılı ve hassas bir düzenleme kontrol sistemi, hücrelerin hücre döngüsünde bir aşamadan diğerine geçme ve mitoza başlama şeklini yönlendirir. Denetim sistemi, hücre içindeki moleküllerin yanı sıra dış tetikleyicileri de içerir. Bu dahili ve harici denetim tetikleyicileri hücre için "dur" ve "ilerle" emirlerini sağlar. Hücre döngüsünün hassas bir şekilde düzenlenmesi, bir organizmanın sağlığını korumak için hayati önem taşır ve hücre döngüsü denetiminin kaybı kansere yol açabilir.
Hücre Döngüsü Denetim Mekanizmaları
Hücre döngüsü boyunca ilerlerken, her aşama hücrenin bir sonraki aşamaya geçmeden önce tamamlanması gereken belirli süreçleri içerir. Denetim noktası, hücre döngüsünde döngünün ilerlemesi veya durdurulması için işaret verilebilen bir noktadır. Bu denetim noktalarının her birinde, hücre içindeki belirli koşullara bağlı olarak farklı molekül çeşitleri dur veya devam işaretlerini sağlar. Siklin, hücre döngüsü kontrol moleküllerinin birincil sınıflarından biridir (aşağıdaki şekil). Sikline bağımlı kinaz (CDK), hücre denetim noktalarını geçerek ilerlemeyi belirlemek için siklinlerle birlikte çalışan bir grup molekülden biridir. Bu tetikleyiciler, birçok ek molekülle etkileşime girerek, -herhangi bir nedenle hücre hazır değilse, "durdurma" sinyalleri tarafından engellenmediği sürece- hücre döngüsünü ileriye doğru iter. G1 kontrol noktasında, hücre DNA sentezinin gerçekleşmesi için hazır olmalıdır. G2 kontrol noktasında hücre mitoz için tamamen hazır olmalıdır. Mitoz sırasında bile, metafazdaki çok önemli bir dur ve devam et denetim noktası, hücrenin hücre bölünmesini tamamlamak için tamamen hazır olmasını sağlar. Metafaz kontrol noktası, anafaz sırasında onları ayırmak için sinyal verilmeden önce tüm kardeş kromatidlerin ilgili mikrotübüllerine düzgün bir şekilde bağlanmasını ve metafaz plakasında sıralanmasını sağlar.
Hücre Döngüsü Kontrolden Çıktığında: Olası Sonuçları
Çoğu insan kanser veya tümörlerin sürekli çoğalan anormal hücrelerden kaynaklandığını bilir. Anormal hücreler durdurulmadan bölünmeye devam ederse, çevrelerindeki dokulara zarar verebilir, vücudun diğer bölgelerine yayılabilir ve sonunda ölümle sonuçlanabilir. Sağlıklı hücrelerde, hücre döngüsünün sıkı düzenleme mekanizmaları bunun olmasını önlerken, hücre döngüsü denetimindeki başarısızlıklar istenmeyen ve aşırı hücre bölünmesine neden olabilir. Denetim başarısızlıkları, belirli "dur" ve " devam et" sinyallerinin işlevini tehlikeye atan kalıtsal genetik bozukluklardan kaynaklanabilir. DNA'ya zarar veren çevresel etkiler de bu sinyallerde işlev bozukluğuna neden olabilir. Genellikle, hem genetik yatkınlık hem de çevresel etkenlerin bir araya gelmesi kansere yol açar.
Bir hücrenin normal kontrol sisteminden kaçarak kansere dönüşmesi süreci aslında vücutta oldukça sık gerçekleşebilir. Neyse ki, bağışıklık sisteminin bazı hücreleri kanserli hale gelen hücreleri tanıma ve onları yok etme yeteneğine sahiptir. Ancak bazı durumlarda kanserli hücreler tespit edilmeden kalır ve çoğalmaya devam eder. Ortaya çıkan tümör çevre dokular için bir tehdit oluşturmuyorsa, iyi huylu olduğu söylenir ve genellikle kolayca çıkarılabilir. Eğer zarar verme kabiliyeti varsa, tümör kötü huylu olarak kabul edilir ve hastaya kanser teşhisi konur.
| HOMEOSTATİK DENGESİZLİKLER Kanser Homeostatik Dengesizliklerden Kaynaklanır Kanser, çok çeşitli genetik ve çevresel nedenlerden kaynaklanabilen son derece karmaşık bir durumdur. Tipik olarak, bir hücrenin DNA’sında normal hücre döngüsü denetim sistemlerini tehlikeye atan mutasyonlar veya sapmalar kanserli tümörlere yol açar. Hücre döngüsü kontrolü, uygun hücre işlevini ve sağlığını koruyan homeostatik bir mekanizma örneğidir. Hücre döngüsünün aşamaları boyunca ilerlerken, çok çeşitli hücre içi moleküller bir sonraki aşamaya ilerlemeyi düzenlemek için dur ve devam et işaretleri sağlar. Bu işaretler karmaşık bir denge içinde tutulur, böylece hücre ancak hazır olduğunda bir sonraki aşamaya geçer. Hücre döngüsünün bu homeostatik kontrolü, bir arabanın hız sabitleyicisi gibi düşünülebilir. Hız sabitleyici, istenen bir hızı korumak için sürekli olarak doğru miktarda ivmelenme uygulayacak, ancak sürücü frenlere bastığında araç yavaşlayacaktır. Benzer şekilde, hücre, döngüsünde hücreyi ileri iten siklinler gibi moleküler haberciler içerir. Siklinlere ek olarak, proto-onkogen adı verilen genler tarafından kodlanan bir protein sınıfı, hücre döngüsünü düzenleyen ve onu ileriye taşıyan önemli sinyaller sağlar. Proto-onkogen ürünlerine örnek olarak büyüme faktörleri için hücre yüzeyi reseptörleri veya DNA kopyalanmasını ve hücre bölünmesini teşvik edebilen iki molekül sınıfı olan hücre sinyal molekülleri verilebilir. Buna karşılık, tümör baskılayıcı genler olarak bilinen ikinci bir gen sınıfı, hücre döngüsü sırasında durdurma sinyalleri gönderir. Örneğin, tümör baskılayıcı genlerin bazı protein ürünleri DNA’daki potansiyel sorunları işaret eder ve böylece hücrenin bölünmesini durdurur, diğer proteinler ise tamir edilemeyecek kadar hasar görürse hücrenin ölmesi için haber verir. Bazı tümör baskılayıcı proteinler de hücrenin şu anda bölünmesine gerek olmadığını gösteren yeterli bir çevresel hücresel yoğunluğa işaret eder. İkinci işlev, tümör büyümesini önlemede benzersiz bir öneme sahiptir: normal hücreler “temas inhibisyonu” adı verilen bir olgu sergiler; bu nedenle, komşu hücrelerle yoğun hücresel temas, daha fazla hücre bölünmesini durduran bir işarete neden olur. Bu iki zıt gen sınıfı, proto-onkogenler ve tümör baskılayıcı genler, sırasıyla hücrenin kendi “hız sabitleme sisteminin” gaz ve fren pedalı gibidir. Normal koşullar altında, bu dur ve git sinyalleri homeostatik bir denge içinde tutulur. Genel olarak, hücrenin hız sabitleyicisinin kontrolü kaybetmesinin iki yolu vardır: arızalı (aşırı aktif) bir gaz pedalı veya arızalı (yetersiz aktif) bir fren. Proto-onkogenler bir mutasyon yoluyla tehlikeye girdiğinde veya başka bir şekilde değiştirildiğinde; bir hücreyi döngüsünde ileri iten ve bunu yapmak istenmediğinde bile hücre bölünmesini uyaran onkoproteinler üreten onkogenlere dönüştürülebilir. Örneğin, yoğun DNA hasarı nedeniyle kendini yok etmeye programlanmış olması gereken bir hücre (apoptoz adı verilen bir süreç) bunun yerine bir onkoprotein tarafından çoğalmaya tetiklenebilir. Öte yandan, işlevsiz bir tümör baskılayıcı gen, hücreye gerekli bir durdurma sinyali sağlayamayabilir ve bu da istenmeyen hücre bölünmesi ve çoğalması ile sonuçlanabilir. Birçok proto-onkogen ve tümör baskılayıcı gen arasındaki hassas bir homeostatik denge, hücre döngüsünü hassas bir şekilde kontrol eder ve yalnızca sağlıklı hücrelerin çoğalmasını sağlar. Bu nedenle, bu homeostatik dengenin bozulması, anormal hücre bölünmesine ve kanserli büyümelere neden olabilir. |
| İNTERAKTİF BAĞLANTI Mitoz bölünme hakkında bilgi edinmek için bu bağlantıyı ziyaret edin. Mitoz bölünme iki özdeş diploid hücre ile sonuçlanır. Profaz sırasında hangi yapılar oluşur? Önceki Ders: Protein Sentezi Sonraki Ders: Hücresel Farklılaşma |



Yorumlar
Yorum Gönder