İnsan İşlevleri için Gerekli Organik Bileşikler
Organik bileşikler tipik olarak hidrojene, genellikle oksijene ve sıklıkla diğer elementlere kovalent olarak bağlanmış karbon atomu gruplarından oluşur. Dünyanın her yerinde, toprakta ve denizlerde, ticari ürünlerde ve insan vücudunun her hücresinde bulunurlar. İnsan yapısı ve işlevi için en önemli dört tür karbonhidratlar, lipidler, proteinler ve nükleik asitlerdir. Bu bileşikleri keşfetmeden önce karbonun kimyasını anlamanız gerekir.
Karbonun Kimyası
Organik bileşiklerin her yerde bulunmasını sağlayan şey, karbon çekirdeklerinin kimyasıdır. Karbon atomlarının değerlik kabuğunda dört elektron olduğunu ve sekizli kuralının, atomların değerlik kabuklarını sekiz elektronla tamamlayacak şekilde reaksiyona girme eğiliminde olduklarını belirttiğini hatırlayın. Karbon atomları dört elektron vererek veya kabul ederek değerlik kabuklarını tamamlamazlar. Bunun yerine, kovalent bağlar aracılığıyla elektronları kolayca paylaşırlar.
Genellikle, karbon atomları diğer karbon atomlarıyla elektronlarını paylaşarak karbon iskeleti olarak adlandırılan uzun bir karbon zinciri oluşturur. Ancak paylaştıklarında, tüm elektronlarını yalnızca birbirleriyle paylaşmazlar. Bunun yerine, karbon atomları elektronları, biri her zaman hidrojen olan çeşitli diğer elementlerle paylaşma eğilimindedir. Karbon ve hidrojen grupları hidrokarbon olarak adlandırılır. Bu bölümün geri kalanında organik bileşiklerin şekillerini incelerseniz, bileşiğin bir bölgesinde hidrokarbon zincirleri içeren birkaç tane göreceksiniz.
Karbon'un dört "boşluğunu" doldurmak için birçok kombinasyon mümkündür. Karbon, organik bir bileşiğin belirli bir bölgesinde elektronları oksijen, azot veya diğer atomlarla paylaşabilir. Ayrıca, karbon atomlarının bağlandığı atomlar da bir fonksiyonel grubun parçası olabilir. Fonksiyonel bir grup, güçlü kovalent bağlarla birbirine bağlanmış ve kimyasal reaksiyonlarda tek bir birim olarak işlev görme eğiliminde olan bir grup atomdur. İşlevsel grupları, üyelerinin ayrılması pek mümkün olmayan, sıkı sıkıya örülmüş "klikler" olarak düşünebilirsiniz. İnsan fizyolojisinde beş işlevsel grup önemlidir; bunlar hidroksil, karboksil, amino, metil ve fosfat gruplarıdır (aşağıdaki tablo).

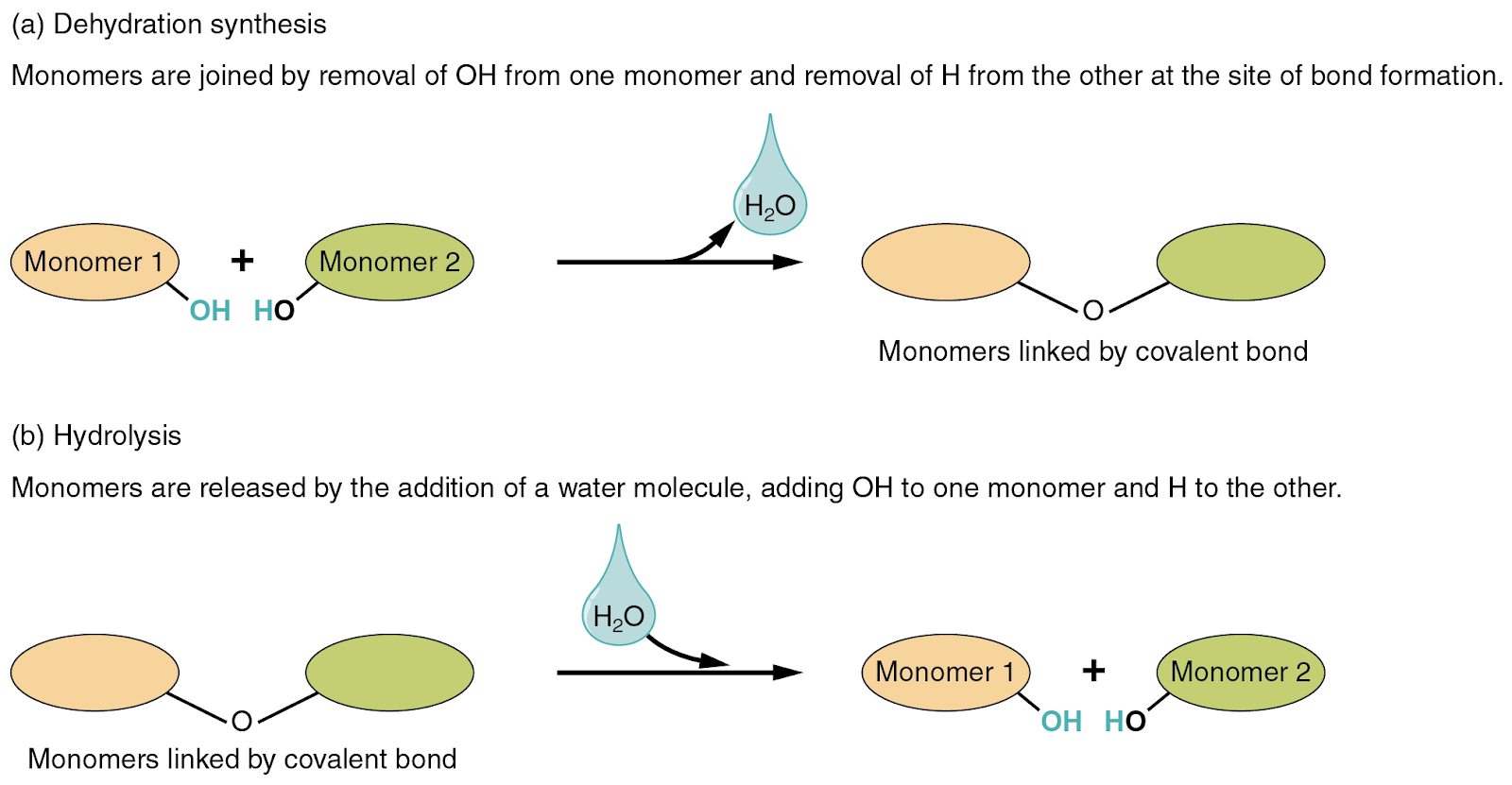
Karbonun kovalent bağlanmaya olan eğilimi, birçok farklı ve nispeten stabil organik molekülün, daha büyük ve karmaşık molekülleri kolaylıkla oluşturmasına neden olur. Herhangi bir büyük molekül makromolekül (makro- = "büyük") olarak adlandırılır ve bu bölümdeki organik bileşiklerin tümü bu tanıma uymaktadır. Ancak bazı makromoleküller, monomer (mono- = "bir"; -mer = "parça") adı verilen tek birimlerin birkaç "kopyasından" oluşur. Uzun bir kolyedeki boncuklar gibi, bu monomerler uzun polimerler (poly- = "birçok") oluşturmak için kovalent bağlarla bağlanır. Organik bileşikler arasında birçok monomer ve polimer örneği bulunmaktadır.
Monomerler dehidrasyon sentezine girerek polimerleri oluşturur (yukarıdaki şekil). Daha önce de belirtildiği gibi, bu reaksiyon bir molekül suyun açığa çıkmasıyla sonuçlanır. Her monomer katkıda bulunur: Biri bir hidrojen atomu ve diğeri bir hidroksil grubu verir. Polimerler hidroliz yoluyla monomerlerine ayrılır (-lysis = "kopma"). Monomerleri arasındaki bağlar, bir monomere bir hidrojen atomu ve diğerine bir hidroksil grubu katan bir su molekülünün bağışlanması yoluyla kırılır.
Karbonhidratlar
Karbonhidrat terimi "hidratlı karbon" anlamına gelir. Hidro- kökünün suyu gösterdiğini hatırlayın. Bir karbonhidrat karbon, hidrojen ve oksijenden oluşan bir moleküldür; çoğu karbonhidratta hidrojen ve oksijen suda sahip oldukları ikiye bir nispi oranlarda bulunur. Aslında, "genel" bir karbonhidrat molekülünün kimyasal formülü (CH2O)n'dir.
Karbonhidratlar, "şekerler" anlamına gelen bir kelime olan sakkaritler olarak adlandırılır. Vücutta üç biçim önemlidir. Monosakkaritler karbonhidratların monomerleridir. Disakkaritler (di- = "iki") iki monomerden oluşur. Polisakkaritler polimerlerdir ve yüzlerce ila binlerce monomerden oluşabilir.
Monosakkaridler
Bir monosakkarit, karbonhidratların bir monomeridir. Beş monosakkarit vücutta önemlidir. Bunlardan üçü, her biri altı karbon atomu içerdiği için bu şekilde adlandırılan heksoz şekerlerdir. Bunlar aşağıdaki şekilde üst görsellerde gösterilen glukoz, fruktoz ve galaktozdur. Geriye kalan monosakkaritler, her biri beş karbon atomu içeren iki pentoz şekeridir. Bunlar aşağıdaki şekilde alt görsellerde gösterilen riboz ve deoksiribozdur.
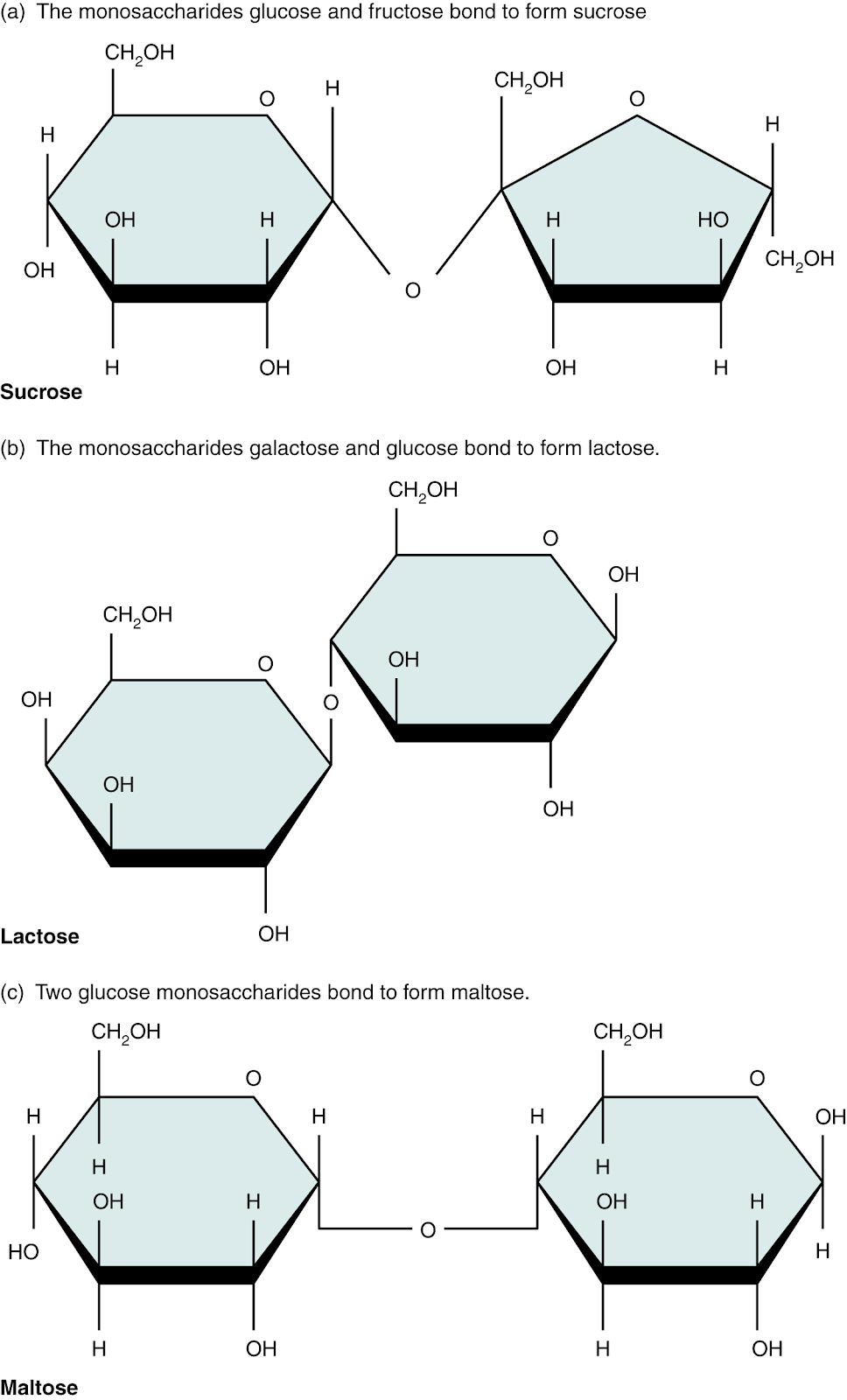
Disakkaridler
Bir disakkarit, bir çift monosakkarittir. Disakkaritler dehidrasyon sentezi yoluyla oluşur ve onları birbirine bağlayan bağa glikozit bağı (gliko- = "şeker") denir. Üç disakkarit (aşağıdaki şekilde gösterilmiştir) insanlar için önemlidir. Bunlar genellikle sofra şekeri olarak adlandırılan sakaroz; laktoz veya süt şekeri; ve maltoz veya arpa şekeridir. Ortak isimlerinden de anlayabileceğiniz gibi, bunları diyetinizde tüketirsiniz; ancak vücudunuz bunları doğrudan kullanamaz. Bunun yerine, sindirim sisteminde hidroliz yoluyla bileşen monosakkaritlerine ayrılırlar.
| İNTERAKTİF BAĞLANTI Bir disakkarit oluşumunu gözlemlemek için bu videoyu izleyin. Su bir glikozit bağıyla karşılaştığında ne olur? |
Polisakkaridler
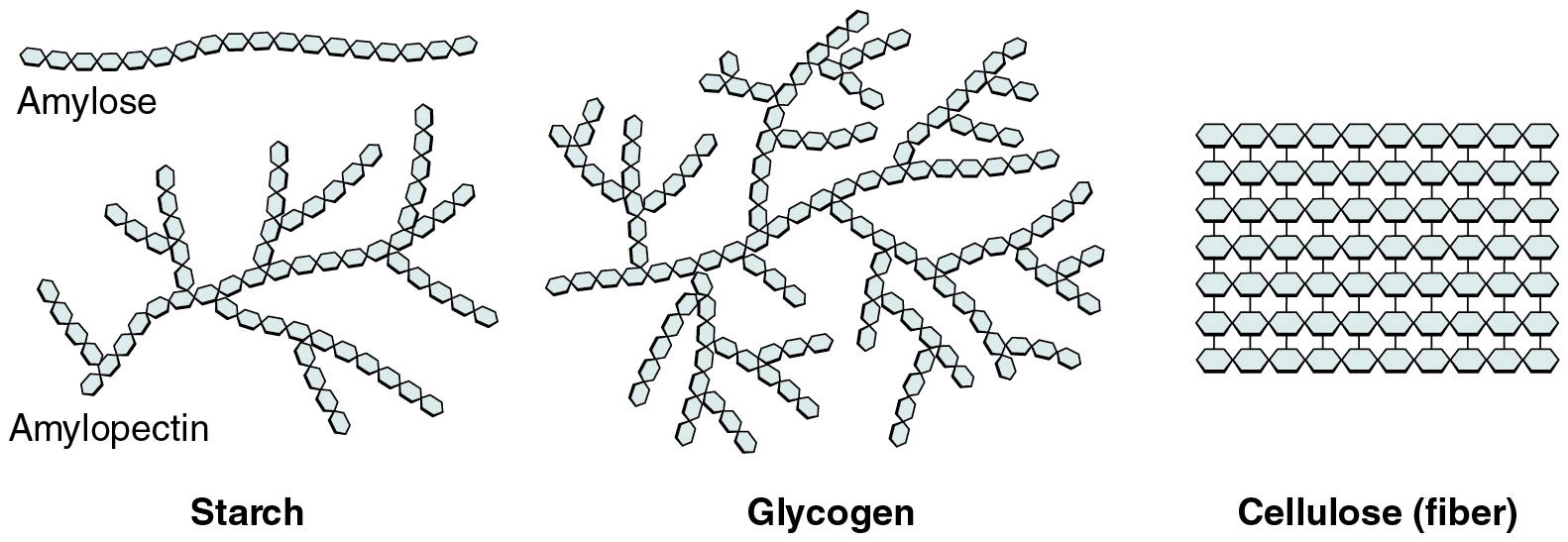
Polisakkaritler birkaç ila bin veya daha fazla monosakkarit içerebilir. Bunlardan üçü vücut için önemlidir (aşağıdaki şekil):
- Nişastalar glukoz polimerleridir. Amiloz adı verilen uzun zincirler veya amilopektin adı verilen dallanmış zincirler halinde bulunurlar ve her ikisi de bitki bazlı gıdalarda depolanır ve sindirimi nispeten kolaydır.
- Glikojen de bir glikoz polimeridir, ancak hayvanların dokularında, özellikle kaslarda ve karaciğerde depolanır. Kesimden sonra hayvan dokularında çok az glikojen kalması nedeniyle, glikojen, besinsel bir karbonhidrat olarak kabul edilmez; ancak insan vücudu, fazla glukozu glikojen olarak kas ve karaciğere depolar.
- Yeşil bitkilerin hücre duvarının birincil bileşeni olan bir polisakkarit olan selüloz, bitkisel gıdanın "lif" olarak adlandırılan bileşenidir. İnsanlarda selüloz/lif sindirilemez; ancak diyet lifinin sağlık açısından birçok faydası vardır. Tok hissetmenize yardımcı olarak daha az yemenizi sağlar, sağlıklı bir sindirim sistemini destekler ve lif oranı yüksek bir diyetin kalp hastalığı ve muhtemelen bazı kanser türleri riskini azalttığı düşünülmektedir.
Karbonhidratların İşlevleri
Vücut karbonhidratları bitki bazlı gıdalardan elde eder. Süt ürünlerinde laktoz bulunmasına rağmen tahıllar, meyveler ve baklagiller ve diğer sebzeler insan beslenmesindeki karbonhidratın çoğunu sağlar.
Çoğu vücut hücresi yakıt için diğer organik bileşikleri parçalayabilse de, tüm vücut hücreleri glikoz kullanabilir. Dahası, beyindeki, omurilikteki ve çevresel sinir sistemindeki sinir hücreleri (nöronlar) ve kırmızı kan hücreleri yakıt olarak yalnızca glikoz kullanabilir. Glikozun enerji için parçalanması sırasında, daha çok ATP olarak bilinen adenozin trifosfat molekülleri üretilir. Adenozin trifosfat (ATP) bir riboz şekeri, bir adenin bazı ve üç fosfat grubundan oluşur. ATP, fosfat bağları koptuğunda serbest enerji açığa çıkarır ve böylece hücreye hazır enerji sağlar. Oksijen (O2) varlığında, oksijen kullanılmayan yollara göre daha fazla ATP üretilir. Glikozdaki enerjinin ATP'de depolanan enerjiye dönüşümü için genel reaksiyon yazılabilir:
Karbonhidratlar kritik bir yakıt kaynağı olmalarının yanı sıra hücrelerin yapısında çok az miktarda bulunurlar. Örneğin, bazı karbonhidrat molekülleri proteinlerle bağlanarak glikoproteinleri, diğerleri ise lipitlerle birleşerek glikolipitleri üretir; bunların her ikisi de vücut hücrelerinin içeriğini çevreleyen zarda bulunur.
Yağlar
Yağ, çoğunlukla hidrokarbonlardan oluşan oldukça çeşitli bir grup bileşikten biridir. İçerdikleri az sayıdaki oksijen atomu genellikle molekülün çevresinde yer alır. Polar olmayan hidrokarbonları sayesinde tüm lipidler hidrofobik halde olurlar. Suda, lipitler gerçek bir çözelti oluşturmazlar; ancak iyi karışmayan çözeltilerin karışımı için kullanılan bir terim olan bir emülsiyon oluşturabilirler.
Trigliseridler
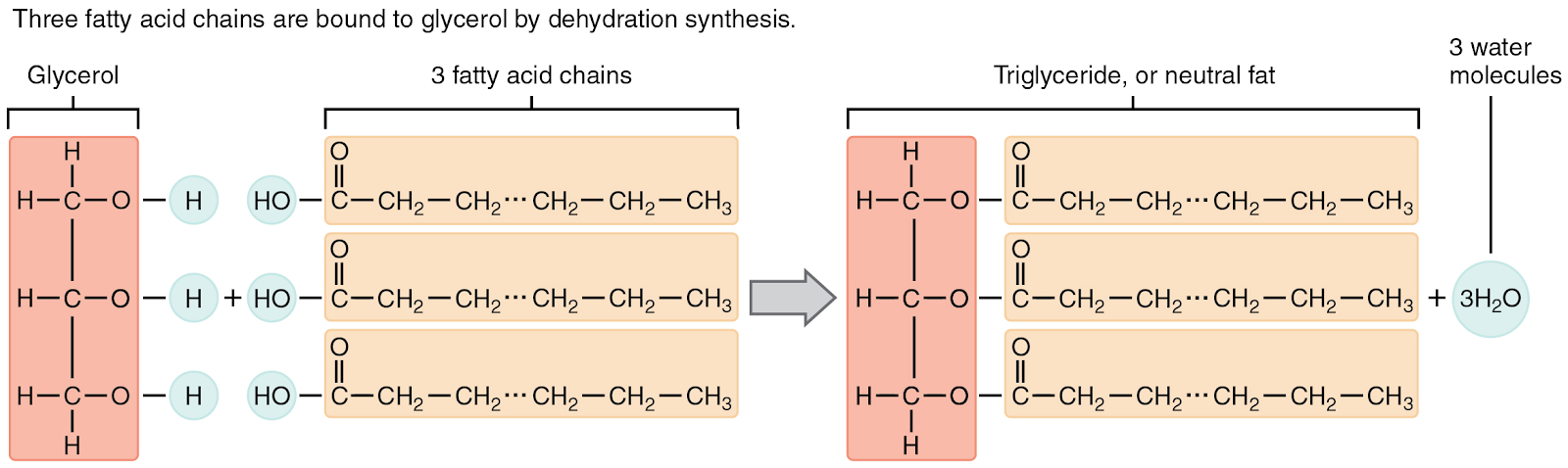
Trigliserit, en yaygın diyet lipit gruplarından biridir ve vücut dokularında en bol bulunan türdür. Genellikle yağ olarak adlandırılan bu bileşik, iki tür molekülün sentezinden oluşur (aşağıdaki şekil):
- Trigliseritlerin çekirdeğinde yer alan gliserol omurgası, üç karbon atomundan oluşur.
- Gliserolün her bir karbonundan, -karboksil grubu ve metil grubu olan uzun hidrokarbon zincirleri bulunan- üç yağ asidi uzanır.
Trigliseritler dehidrasyon sentezi yoluyla oluşur. Gliserol, her bağdaki hidroksil gruplarından hidrojen atomları bırakır ve her yağ asidi zincirindeki karboksil grubu bir hidroksil grubunu bırakır. Böylece toplam üç su molekülü serbest kalır.
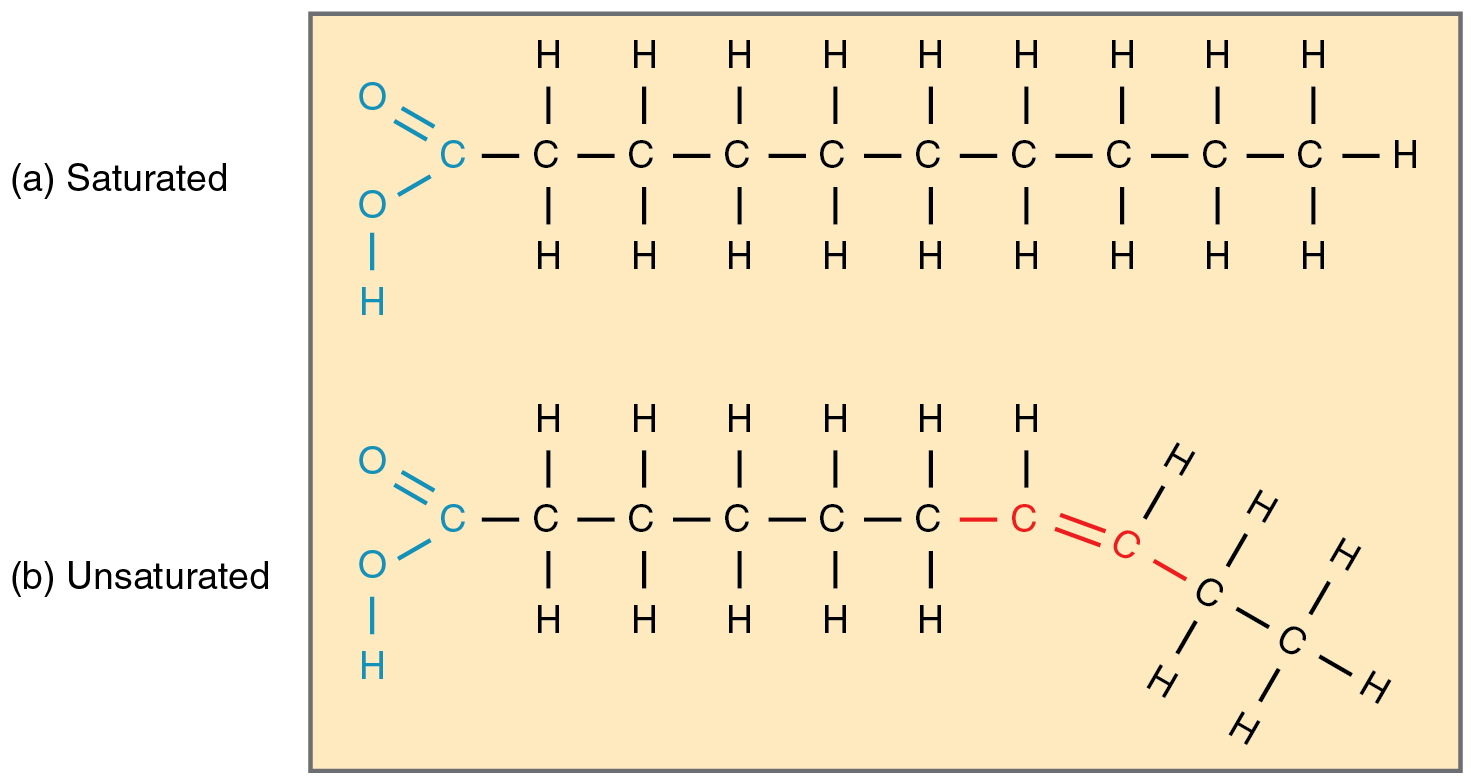
Uzunlukları boyunca hiçbir yerde çift karbon bağı bulunmayan ve bu nedenle maksimum sayıda hidrojen atomu içeren yağ asidi zincirlerine doymuş yağ asitleri denir. Bu düz, sert zincirler sıkıca bir araya gelir ve oda sıcaklığında katı veya yarı katıdır (aşağıdaki şeklin yukarısındaki görseli). Tereyağı ve domuz yağı, biftekte veya kendi vücudunuzda bulunan yağ gibi örneklerdir. Buna karşılık, bir adet çift karbon bağı olan yağ asitleri o bağda bükülmüştür (aşağıdaki şeklin aşağısındaki görseli). Bu tekli doymamış yağ asitleri bu nedenle sıkıca bir araya gelemezler ve oda sıcaklığında sıvı haldedirler. Çoklu doymamış yağ asitleri iki veya daha fazla çift karbon bağı içerir ve oda sıcaklığında da sıvıdır. Zeytinyağı gibi bitkisel yağlar tipik olarak hem tekli hem de çoklu doymamış yağ asitleri içerir.
Doymuş yağ asitleri bakımından yüksek bir diyet kalp hastalığı riskini artırırken, doymamış yağ asitleri bakımından yüksek bir diyetin riski azalttığı düşünülmektedir. Bu durum özellikle somon gibi soğuk su balıklarında bulunan omega-3 doymamış yağ asitleri için geçerlidir. Bu yağ asitlerinin ilk çift karbon bağı metil grubundan sonraki üçüncü hidrokarbonda bulunur (molekülün omega ucu olarak adlandırılır).
Son olarak, bazı çubuk ve tüp margarinler de dahil olmak üzere bazı işlenmiş gıdalarda bulunan trans yağ asitlerinin kalp ve kan damarları için doymuş yağ asitlerinden bile daha zararlı olduğu düşünülmektedir. Trans yağlar, doymamış yağ asitlerinden (mısır yağı gibi) kısmen hidrojenize yağlar üretmek için kimyasal işlemden geçirilerek oluşturulur.
Bir grup olarak trigliseritler vücut için önemli bir yakıt kaynağıdır. Dinlenirken veya uyurken, hayatta kalmanızı sağlamak için kullanılan enerjinin büyük bir kısmı yağ (adipoz) dokularınızda depolanan trigliseritlerden elde edilir. Trigliseridler ayrıca bahçe işleri veya yürüyüş gibi uzun ve yavaş fiziksel aktiviteleri besler ve şiddetli fiziksel aktiviteler için mütevazı bir enerji yüzdesine katkıda bulunur. Diyet yağı ayrıca polar olmayan yağda çözünen A, D, E ve K vitaminlerinin emilimine ve taşınmasına yardımcı olur. Ayrıca, depolanan vücut yağı vücudun kemiklerini ve iç organlarını korur ve yastıklar ve vücut ısısını korumak için yalıtım görevi görür.
Yağ asitleri aynı zamanda hücre zarında bulunan şeker-yağ bileşikleri olan glikolipidlerin de bileşenleridir. Lipoproteinler, hidrofobik trigliseritlerin vücut sıvılarında taşınmak üzere protein zarflar içinde paketlendiği bileşiklerdir.
Fosfolipidler
Adından da anlaşılacağı üzere fosfolipid, bir lipidin gliserol bileşeni ile bir fosfor molekülü arasındaki bağdır. Aslında fosfolipidler yapı olarak trigliseridlere benzer. Bununla birlikte, üç yağ asidi yerine, sadece iki yağ asidi zinciri olan bir gliserol olan bir digliseritten bir fosfolipid üretilir (aşağıdaki şekil). Gliserol üzerindeki üçüncü bağlanma bölgesi fosfat grubu tarafından alınır ve bu da molekülün polar bir "baş" bölgesine bağlanır. Trigliseritlerin polar olmadığını ve hidrofobik olduğunu hatırlayın. Bu durum fosfolipid bileşiğinin yağ asidi kısmı için de geçerlidir. Bununla birlikte, bir fosfolipidin başı, fosfat gruplarının yanı sıra azot atomu üzerinde de yükler içerir. Bu yükler fosfolipid başını hidrofilik hale getirir. Bu nedenle, fosfolipidlerin nötr yağ asitlerini içeren hidrofobik kuyruklara ve yüklü fosfat gruplarını ve azot atomunu içeren hidrofilik başlara sahip olduğu söylenir.
Steroidler
Bir steroid bileşiği (sterol olarak adlandırılır) temel olarak çeşitli diğer atomlara ve moleküllere bağlanmış dört hidrokarbon halkasına sahiptir (yukarıdaki şeklin ortasındaki görseli). Hem bitkiler hem de hayvanlar sterol sentezlese de, insan yapısına ve işlevine en önemli katkıyı yapan tür, insanlarda ve hayvanlarda karaciğer tarafından sentezlenen ve çoğu hayvansal gıdada da bulunan kolesteroldür. Diğer lipidler gibi, kolesterolün hidrokarbonları onu hidrofobik yapar; ancak, hidrofilik olan polar bir hidroksil başlığına sahiptir. Kolesterol, diyet yağlarını emülsifiye etmeye yardımcı olan bileşikler olan safra asitlerinin önemli bir bileşenidir. Aslında chole- kelime kökü safra anlamına gelir. Kolesterol aynı zamanda -vücudun uzak bölgelerdeki süreçleri düzenlemek için salgıladığı sinyal molekülleri olan- birçok hormonun yapı taşıdır. Son olarak, fosfolipitler gibi kolesterol molekülleri de hücre zarında bulunur, hidrofobik ve hidrofilik bölgeleri sayesinde hücreye giren ve hücreden çıkan maddelerin akışını düzenlemeye yardımcı olurlar.
Prostaglandinler
Bir hormon gibi, bir prostaglandin de bir grup sinyal molekülünden biridir, ancak prostaglandinler doymamış yağ asitlerinden türetilir (yukarıdaki şeklin aşağısındaki görseli). Balıkta bulunan omega-3 yağ asitlerinin faydalı olmasının bir nedeni, kan basıncı ve iltihaplanma yönlerini düzenlemeye yardımcı olan belirli prostaglandinlerin üretimini uyarması ve böylece kalp hastalığı riskini azaltmasıdır. Prostaglandinler ayrıca sinirleri ağrıya karşı hassaslaştırır. Nonsteroid antienflamatuar ilaçlar (NSAID'ler) olarak adlandırılan bir ağrı kesici ilaç sınıfı, prostaglandinlerin etkilerini azaltarak çalışır.
Proteinler
Proteinleri kas dokusu ile ilişkilendirebilirsiniz, ancak aslında proteinler tüm doku ve organların kritik bileşenleridir. Protein, peptit bağlarıyla birbirine bağlanmış amino asitlerden oluşan organik bir moleküldür. Proteinler arasında cildin epidermisinde bulunan ve alttaki dokuları koruyan keratin, cildin dermisinde, kemiklerde ve beyin ile omuriliği kaplayan meninkslerde bulunan kolajen yer alır. Proteinler aynı zamanda sindirim sistemindeki sindirim enzimleri, antikorlar, nöronların diğer hücrelerle iletişim kurmak için kullandığı nörotransmiterler ve belirli vücut fonksiyonlarını düzenleyen peptit bazlı hormonlar (örneğin büyüme hormonu) dahil olmak üzere vücudun işlevsel kimyasallarının çoğunun bileşenleridir. Karbonhidratlar ve lipidler hidrokarbonlar ve oksijenden oluşurken, tüm proteinler karbon, hidrojen ve oksijene ek olarak azot (N) ve birçoğu da sülfür (S) içerir.
Proteinlerin Mikroyapısı
Proteinler, amino asit adı verilen azot içeren monomerlerden oluşan polimerlerdir. Bir amino asit, değişken bir yan zincirle birlikte bir amino grubu ve bir karboksil grubundan oluşan bir moleküldür. Sadece 20 farklı amino asit, insan yapısı ve işlevinde önemli olan binlerce farklı proteinin neredeyse tamamına katkıda bulunur. Vücut proteinleri, bu 20 amino asit monomerinin birkaç düzine ila birkaç yüzünün benzersiz bir kombinasyonunu içerir. Bu amino asitlerin 20'si de benzer bir yapıya sahiptir (aşağıdaki şekil). Hepsi, aşağıdakilerin bağlı olduğu merkezi bir karbon atomundan oluşur:
- bir hidrojen atomu
- bir alkalin (bazik) amino grubu NH2 (yukarıdaki tablo)
- asidik bir karboksil grubu COOH (yukarıdaki tablo)
- değişken bir grup
Tüm amino asitlerin hem bir asit (karboksil grubu) hem de bir baz (amino grubu) içerdiğine dikkat edin (amin = "azot içeren"). Bu nedenle mükemmel tamponlar oluşturarak vücudun asit-baz dengesini düzenlemesine yardımcı olurlar. Bu 20 amino asidi birbirinden ayıran şey, yan zincir ya da R grubu olarak adlandırılan değişken gruplarıdır. Bu grup boyut olarak değişebilir ve polar veya polar olmayan olabilir, bunlar da her amino aside benzersiz özellikler kazandırır. Örneğin, iki amino asidin -sistein ve metiyonin- yan zincirleri sülfür içerir. Sülfür hidrojen bağlarına kolaylıkla katılmazken, diğer tüm amino asitler katılır. Bu varyasyon, sistein ve metiyonin içeren proteinlerin bir araya gelme şeklini etkiler.
Amino asitler dehidrasyon sentezi yoluyla birleşerek protein polimerlerini oluştururlar (aşağıdaki şekil). Amino asitleri bir arada tutan eşsiz bağa peptit bağı denir. Bir peptit bağı, iki amino asit arasında dehidrasyon sentezi ile oluşan kovalent bir bağdır. Aslında bir peptit, amino asitlerden oluşan çok kısa bir zincirdir. Yaklaşık 100 amino asitten daha az amino asit içeren iplikçikler genellikle protein yerine polipeptit olarak adlandırılır.
Vücut amino asitlerin çoğunu diğer moleküllerin bileşenlerinden sentezleyebilir; ancak dokuz tanesi sentezlenemez ve diyetle tüketilmesi gerekir. Bunlar esansiyel amino asitler olarak bilinir.
Protein yapımı için mevcut olan serbest amino asitlerin hücrelerdeki amino asit havuzunda bulunduğu söylenir. Hücrelerdeki yapılar proteinleri bir araya getirirken bu amino asitleri kullanır. Bununla birlikte, belirli bir esansiyel amino asit, amino asit havuzunda yeterli miktarlarda mevcut değilse, onu içeren proteinlerin sentezi yavaşlayabilir veya hatta durabilir.
Proteinlerin Şekli
Nasıl ki çorba içmek için çatal, et yemek için kaşık kullanılamazsa, bir proteinin şekli de işlevi için gereklidir. Bir proteinin şekli, en temelde, yapıldığı amino asitlerin dizilimi tarafından belirlenir (aşağıdaki şeklin yukarısındaki görseli). Bu dizilime proteinin birincil yapısı denir.
Bazı polipeptitler düz zincirler halinde var olsa da, çoğu, polipeptitin farklı bölgelerinde farklı özelliklere sahip amino asitler arasında bağlanma gerçekleştiğinde oluşan daha kompleks ikincil yapılarla bükülmüş veya katlanmıştır. En yaygın ikincil yapı, alfa sarmal adı verilen bir spiraldir. Eğer bir ipi alıp basitçe spiral şeklinde bükecek olsaydınız, şeklini koruyamazdı. Benzer şekilde, amino asitlerden oluşan bir iplikçik, aynı iplikçiğin farklı bölgeleri arasında köprüler oluşturan hidrojen bağlarının yardımı olmadan istikrarlı bir spiral şekli koruyamaz (yukarıdaki şeklin ortasındaki görsel). Daha az yaygın olarak, bir polipeptit zinciri, hidrojen bağlarının kendi üzerine katlanmış tek bir polipeptidin farklı bölgeleri arasında veya iki veya daha fazla bitişik polipeptit zinciri arasında köprüler oluşturduğu beta kıvrımlı bir tabaka oluşturabilir.
Proteinlerin ikincil yapısı, proteinin üçüncül yapısı olarak adlandırılan kompakt bir üç boyutlu şekle daha da katlanır (yukarıdaki şeklin aşağısındaki görseli). Bu konfigürasyonda, birincil zincirde çok uzak olan amino asitler hidrojen bağları veya sistein içeren proteinlerde disülfit bağları yoluyla oldukça yakınlaştırılabilir. Disülfit bağı, bir polipeptitteki sülfür atomları arasındaki kovalent bir bağdır. Genellikle iki veya daha fazla ayrı polipeptit birleşerek kuaterner yapıya sahip daha büyük bir protein oluşturur (yukarıdaki şeklin sağ aşağısındaki görseli). Kuaterner yapıyı oluşturan polipeptit alt birimleri aynı veya farklı olabilir. Örneğin, kırmızı kan hücrelerinde bulunan protein olan hemoglobin, ikisi alfa zinciri ve ikisi beta zinciri olarak adlandırılan dört üçüncül polipeptitten oluşur.
Proteinler aşırı ısıya, asitlere, bazlara ve diğer bazı maddelere maruz kaldıklarında denatüre olurlar. Denatürasyon, fiziksel veya kimyasal yollarla bir molekülün yapısında meydana gelen değişikliktir. Denatüre proteinler işlevsel şekillerini kaybeder ve artık görevlerini yerine getiremezler. Protein denatürasyonunun günlük bir örneği, asidik limon suyu eklendiğinde sütün kesilmesidir.
Bir proteinin şeklinin işlevine katkısı çok önemlidir. Örneğin, kas dokusunu oluşturan protein iplikçiklerinin uzun, ince şekli, kasılma (kısalma) ve gevşeme (uzama) yetenekleri için gereklidir. Başka bir örnek olarak, kemikler, kemik minerallerinin biriktiği iskele görevi gören kolajen adı verilen bir proteinden uzun iplikler içerir. Lifli proteinler olarak adlandırılan bu uzun proteinler güçlü ve dayanıklıdır ve tipik olarak hidrofobiktir.
Buna karşılık, globüler proteinler yüksek oranda tepkisel olma eğiliminde olan ve hidrofilik olan küre veya kürelerdir. Kırmızı kan hücrelerinde bulunan hemoglobin proteinleri buna bir örnektir (yukarıdaki şeklin sağ altındaki görsel); bununla birlikte, globüler proteinler vücudun her yerinde bol miktarda bulunur ve çoğu vücut fonksiyonunda kritik rol oynar. Daha önce protein katalizörleri olarak tanıtılan enzimler buna örnektir. Bir sonraki bölümde enzimlerin etkisine daha yakından bakılacaktır.
Proteinler Enzim Olarak İşlev Görür
Bir makale yazmaya çalışıyor olsaydınız ve dizüstü bilgisayarınızda bir tuşa her bastığınızda yanıt almadan önce altı veya yedi dakikalık bir gecikme yaşasaydınız, muhtemelen yeni bir dizüstü bilgisayar alırdınız. Benzer bir şekilde, kimyasal reaksiyonları katalize eden enzimler olmasaydı, insan vücudu işlevsiz kalırdı. İnsan vücudu sadece enzimler işlev gördüğü için çalışır.
Enzimatik tepkimeler -enzimler tarafından katalize edilen kimyasal tepkimeler- substratlar enzime bağlandığında başlar. Bir substrat, enzimatik bir tepkimede bir tepkimeye giren maddedir. Bu, enzimin etkin bölgeler olarak bilinen bölgelerinde meydana gelir (aşağıdaki şekil). Herhangi bir enzim sadece bir tür kimyasal tepkimeyi katalize eder. Özgüllük olarak adlandırılan bu özellik, belirli bir şekle ve elektrik yüküne sahip bir substratın yalnızca o substrata karşılık gelen bir etkin bölgeye bağlanabilmesinden kaynaklanmaktadır.
Bir enzim ve substratları arasındaki bu puzzle benzeri eşleşme nedeniyle, enzimler özgüllükleriyle bilinirler. Aslında, bir enzim substrat(lar)ına bağlandıkça, enzim yapısı geçiş durumu (substrat ve ürün arasındaki yapısal bir ara madde) ile aktif bölge arasında en iyi uyumu bulmak için hafifçe değişir, tıpkı bir lastik eldivenin içine sokulan bir ele göre kalıplanması gibi. Substrat varlığında bu aktif bölge değişikliği, geçiş durumunun eşzamanlı oluşumu ile birlikte tetiklenmiş uyum olarak adlandırılır. Genel olarak, her substrat ve dolayısıyla her kimyasal tepkime için özel olarak eşleşen bir enzim vardır; ancak bazı esneklikler de mevcuttur. Bazı enzimler, yapısal olarak ilişkili birkaç farklı substrat üzerinde hareket etme yeteneğine sahiptir.
Bir substratın bağlanması bir enzim-substrat kompleksi oluşturur. Enzimlerin kimyasal reaksiyonları kısmen hızlandırması muhtemeldir çünkü enzim-substrat kompleksi, substratların etkileşimlerini kolaylaştırmak için en uygun konumda birbirlerine doğru yönelmelerine neden olan bir dizi geçici ve tersine çevrilebilir değişikliğe uğrar. Bu, tepkime hızının artmasını sağlar. Enzim daha sonra ürün(ler)i serbest bırakır ve orijinal şekline geri döner. Enzim daha sonra tekrar sürece dahil olmakta serbesttir ve substrat kaldığı sürece bunu yapacaktır.
Proteinlerin Diğer İşlevleri
Protein barları, tozları ve karışımlarının reklamları, proteinin kas dokusu oluşturmak, onarmak ve korumak için önemli olduğunu söyler, ancak gerçek şu ki proteinler deriden beyin hücrelerine kadar tüm vücut dokularına katkıda bulunur. Ayrıca, bazı proteinler vücut fonksiyonlarını düzenlemeye yardımcı olan kimyasal haberciler olan hormonlar gibi davranır, Örneğin, büyüme hormonu diğer rollerinin yanı sıra iskelet büyümesi için önemlidir.
Daha önce de belirtildiği gibi, bazik ve asidik bileşenler proteinlerin asit-baz dengesinin korunmasında tampon görevi görmesini sağlar, ancak aynı zamanda proteinler sıvı-elektrolit dengesinin düzenlenmesine de yardımcı olurlar. Proteinler sıvıyı çeker ve kanda, hücrelerde ve hücreler arasındaki boşluklarda sağlıklı bir protein konsantrasyonu, bu çeşitli "bölmelerde" sıvı dengesinin sağlanmasına yardımcı olur. Ayrıca, hücre zarındaki proteinler elektrolitlerin hücre içine ve dışına taşınmasına yardımcı olarak bu iyonları sağlıklı bir dengede tutar. Yağlar gibi proteinler de karbonhidratlarla bağlanabilir. Böylece her ikisi de vücutta birçok işleve sahip olan glikoproteinler veya proteoglikanlar üretebilirler.
Karbonhidrat ve yağ alımı yetersiz olduğunda ve glikojen ve yağ dokusu depoları tükendiğinde vücut enerji için proteinleri kullanabilir. Ancak, işlevsel dokular dışında protein için bir depolama alanı olmadığından, proteinin enerji için kullanılması doku yıkımına neden olur ve vücut israfıyla sonuçlanır.
Nükleotidler
İnsan yapısı ve işlevi için önemli olan dördüncü organik bileşik türü nükleotidlerdir (aşağıdaki şekil). Bir nükleotid, üç alt birimden oluşan bir organik bileşik sınıfından biridir:
- bir veya daha fazla fosfat grubu
- bir pentoz şekeri: ya deoksiriboz ya da riboz
- azot içeren bir baz: adenin, sitozin, guanin, timin veya urasil
Nükleotidler nükleik asitlere (DNA veya RNA) veya enerji bileşiği adenozin trifosfata birleştirilebilir.
Nükleik Asitler
Nükleik asitler pentoz şeker türlerine göre farklılık gösterir. Deoksiribonükleik asit (DNA) genetik bilgiyi depolayan nükleotittir. DNA deoksiriboz (ribozdan bir atom daha az oksijene sahip olduğu için böyle adlandırılır) artı bir fosfat grubu ve bir azot içeren baz içerir. DNA için baz "seçenekleri" adenin, sitozin, guanin ve timin'dir. Ribonükleik asit (RNA), genetik kodun protein olarak ortaya çıkmasına yardımcı olan riboz içeren bir nükleotittir. RNA riboz, bir fosfat grubu ve bir azot içeren baz içerir, ancak RNA için baz "seçenekleri" adenin, sitozin, guanin ve urasildir.
Azot içeren bazlar olan adenin ve guanin pürinler olarak sınıflandırılır. Bir pürin, birkaç azot atomu barındıran çift halka yapısına sahip azot içeren bir moleküldür. Sitozin, timin (sadece DNA'da bulunur) ve urasil (sadece RNA'da bulunur) bazları piramidinlerdir. Piramidin, tek bir halka yapısına sahip azot içeren bir bazdır.
Dehidrasyon sentezi ile oluşan bağlar, bir nükleik asit monomerinin pentoz şekerinin bir diğerinin fosfat grubuyla birleşmesiyle "omurga" oluşturur, bu omurgadan azot içeren bileşenlerin bazları, omurgadan dışarı doğru uzanır. DNA'da bu tür iki omurga, hidrojen bağları aracılığıyla birbirlerinin çıkıntılı bazlarına bağlanır. Bunlar çift sarmal olarak bilinen bir şekil oluşturmak üzere bükülürler (aşağıdaki şekil). Bir DNA ipliği içindeki azot içeren bazlar dizisi, hücrelere amino asitlerin proteinler halinde bir araya getirilmesi talimatını veren moleküler bir kod görevi gören genleri oluşturur. İnsanların DNA'larında, her bir hücrenin çekirdeğindeki 46 kromozomda (gelişim sırasında çekirdeklerini kaybeden kırmızı kan hücreleri hariç) kilitli yaklaşık 22.000 gen bulunmaktadır. Bu genler kişinin vücudunu oluşturan genetik kodu taşır ve tek yumurta ikizleri hariç her birey için benzersizdir.
Buna karşılık RNA, bazlarla bezeli tek bir şeker-fosfat omurgasından oluşur. Haberci RNA (mRNA), protein sentezi sırasında DNA'dan gelen genetik talimatları hücrenin sitoplazmadaki protein üretim tesisleri olan ribozomlara taşımak için oluşturulur.
Adenozin Trifosfat
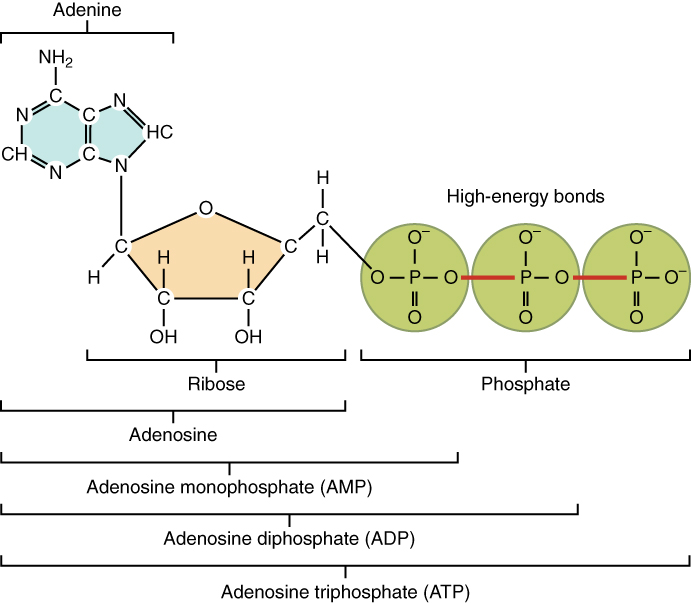
Nükleotid adenozin trifosfat (ATP), bir riboz şekeri, bir adenin bazı ve üç fosfat grubundan oluşur (aşağıdaki şekil). ATP yüksek enerjili bir bileşik olarak sınıflandırılır çünkü üç fosfatını birbirine bağlayan iki kovalent bağ önemli miktarda potansiyel enerji depolar. Vücutta, bu yüksek enerji bağlarından salınan enerji, kas kasılmasından maddelerin hücrelerin içine ve dışına taşınmasına ve anabolik kimyasal reaksiyonlara kadar vücudun faaliyetlerini beslemeye yardımcı olur.
ATP'den bir fosfat grubu ayrıldığında, ürünler adenozin difosfat (ADP) ve inorganik fosfattır (Pi). Bu hidroliz reaksiyonu yazılabilir:

İkinci bir fosfatın çıkarılmasıyla geriye adenozin monofosfat (AMP) ve iki fosfat grubu kalır. Yine bu tepkimeler fosfat-fosfat bağlarında depolanmış olan enerjiyi de serbest bırakır. ADP'nin fosforilasyona uğradığında olduğu gibi bunlar da tersine çevrilebilir. Fosforilleme, organik bir bileşiğe bir fosfat grubunun eklenmesidir, bu durumda ATP'nin oluşması ile sonuçlanır. Bu gibi durumlarda, hidroliz sırasında açığa çıkan aynı seviyedeki enerjinin dehidrasyon sentezine güç sağlamak için yeniden yatırılması gerekir.
Hücreler ayrıca bir fosfat grubunu ATP'den başka bir organik bileşiğe aktarabilir. Örneğin, glikoz bir hücreye ilk girdiğinde, ATP'den bir fosfat grubu transfer edilerek glikoz fosfat (C6H12O6-P) ve ADP oluşturulur. Glikoz bu şekilde fosforile edildikten sonra glikojen olarak depolanabilir veya anında enerji için metabolize edilebilir.
Önceki Ders: İnsan İşlevleri için Gerekli İnorganik Bileşikler
Sonraki Ders: Organizasyonun Kimyasal Seviyesi Bölüm Değerlendirmesi










Yorumlar
Yorum Gönder